新的类胚胎模型模拟早期人类血液生产
匹兹堡大学研究人员开发了一种源自成体细胞的新胚胎样模型,该模型复制了早期人类发育的关键特征,包括血细胞的生成。
今天在《自然》杂志上进行了描述Nature,新的 heX 胚胎模型为了解早期人类提供了一个独特的窗口由于研究这一生命时期的伦理和技术挑战,这一发展一直笼罩在神秘之中。 HeX-Embryoids 不使用胎儿组织,也不能发育成胚胎,可以加强对遗传疾病和不孕症的研究,并使细胞替代或修复组织,用于再生医学应用。
“人类胚胎——与其他物种的胚胎不同,包括一些与我们关系最近的灵长类动物——会嵌入子宫壁中继续发育。由于胚胎比缝衣针的尖端还小,并且隐藏在视野之外,因此这些早期阶段很难研究,”资深作者 Mo Ebrahimkhani说,医学博士,病理学系、匹兹堡肝脏研究所和生物工程系副教授 在皮特。 “我们的类胚胎模型将解开人类发育的&luo;黑匣子&ruo;,这可能有助于解开为什么大约 60% 的怀孕在前两周内失败的谜团——在母亲甚至错过月经之前——并铺平道路。寻找新疗法。”
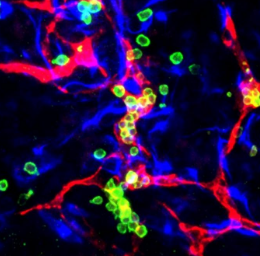
值得注意的是,六角胚胎模型形成的结构与第一个产生血细胞的位点相似,血细胞支持发育中的胚胎,称为血岛。研究人员还检测了红细胞、血小板和不同类型白细胞的祖细胞。 Ebrahimkhani 表示,血细胞的产生是胚胎模型的一个关键进步,推动了该领域的发展。
“我们能够建立与人类血液生成的最早阶段极其相似的模型,”Ebrahimkhani 说,他也是匹兹堡肝脏研究中心的成员 a>。 “这令人兴奋,因为应用该模型有广泛的可能性,可以更好地了解血液是如何形成的,并开发更好的方法来培养用于输血、新型细胞疗法和造血干细胞移植的细胞。”麦高恩再生医学研究所 以及皮特大学和 UPMC 的
为了开发 heX 胚胎,研究人员从诱导多能干细胞 (iPSC) 开始,这些干细胞是由已恢复到可以发育成任何其他细胞的状态的成体细胞产生的。然后,他们用指导早期组织发育的遗传电路对 iPSC 进行了编程,该电路只能由一种名为多西环素的化学物质开启。当这些工程 iPSC 与标准 iPSC 在实验室培养皿中混合并通过添加多西环素进行诱导时,工程细胞会生长并触发标准 iPSC 组织成类似于胚胎某些特征的三维结构。
在正常的胚胎发育中,细胞反复分类和分裂,最终形成不同的部分:滋养层(将成为胎盘)、胚胎外细胞层(产生提供营养的卵黄囊)和胚胎层(产生胚胎)本身和保护发育中的胚胎的羊膜囊。
像胚胎一样,heX-Embryoids 具有胚胎组织和卵黄囊结构。当组织生长时,它仍然固定在实验室培养皿上,形成一大片卵黄囊,其中有数十个并排的胚状体。
“卵黄囊并不直接参与制造形成胚胎的细胞,但它是一个非常重要的组织,因为它负责营养并影响胚胎头部和尾部的位置,”该研究的主要作者约书亚·希斯洛普 (Joshua Hislop) 说道。皮特大学易卜拉欣哈尼实验室的研究生。 “其他类胚胎模型的卵黄囊组织分化非常有限,因此我们的模型提供了一个独特的机会来有力地跟踪这种结构并研究血液发育等事件。”
HeX 胚胎不包含形成胎盘的滋养层,并且卵黄囊是开放的,而不是封闭的腔。缺乏这些特征会阻碍胚胎成为真正的胚胎或无法被植入并完全发育。
由于 heX 胚胎源自重新编程的成人皮肤细胞,因此理论上它们可以由任何个体制成,从而使研究人员能够研究不同的遗传背景。
与其他类胚胎模型相比,heX-Embryoid 系统的一个重要优势在于,它在从二维实验室培养皿中生长时会进行自组织,使用标准生长介质并由单一化学物质启动,而不是依赖于生长因子的复杂混合物可能难以复制。 Ebrahimkhani 表示,这种独特的方法意味着 heX-Embryoids 可以轻松地在不同的实验室中高效地储存、运输和生长。
“对于一个被科学界采用并为新发现做出贡献的模型来说,它必须是高效的,”易卜拉欣哈尼说。 “例如,如果模型本身大部分时间都失败,那么在流产研究方面就很难取得进展。我们的 heX-Embryoid 模型克服了这个问题。”
免责声明:本答案或内容为用户上传,不代表本网观点。其原创性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本站不作任何保证或承诺,请读者仅作参考,并请自行核实相关内容。 如遇侵权请及时联系本站删除。
